Introducere
Infarctul miocardic acut (IMA) reprezintă una dintre cele mai grave patologii cardiovasculare cu morbiditate și mortalitate în creștere [2]. În SUA, anual se depistează circa 1,5 mil. cazuri de IMA, 600 de cazuri la 100.000 de bărbați și 200 la 100.000 femei [1]. În România, anual se înregistrează 13.000 cazuri de IMA, iar în Republica Moldova incidența maladiei constituie 79,1 la 100.000 de locuitori [2, 5]. Rata mortalităţii prin IMA este de 30% în România, 14,7% în SUA, iar în Republica Moldova letalitatea constituie 43,1la 100.000 populație [2, 5].
O complicație majoră a IMA este șocul cardiogen (ȘC), deseori însoțit de dereglări de ritm și conductibilitate, care în unele surse de literatură este supranumit șoc aritmogen. În SUA, la pacienții cu IMA, incidența ȘC variază de la 5 la 10%, iar rata mortalității constituie 80-90% [2, 6]. Studiile recente din SUA raportează micșorarea letalității intraspitalicești la pacienții cu ȘC până la 56-67%, acest fapt fiind explicat prin terapia trombolitică, procedurile intervenționale coronariene (PTCA), terapia insuficienței cardiace cu preparate noi inotrope – levosimendan [1, 4].
Tulburările de ritm în IM survin tranzitoriu, fugace în aproximativ 90% din cazuri, preponderent în faza supraacută a IMA, în decursul primelor ore ale procesului. În literatura de referință sunt relatate modificări ECG ale disritmiilor în 36% (de la 9 până la 80%) cazuri, condiționate de aritmogeneza metabolică, hemodinamică, structural anatomică și prin modificarea tonusului neurovegetativ [4, 6]. IMA poate debuta cu tahicardie ventriculară (TV), fibrilaţie ventriculară (FV), sau bloc atrioventricular (BAV) complet, cauza principală de moarte subită cardiacă (MCS). FV sau TV susţinută se depistează la 20% din pacienţii diagnosticaţi cu STEMI cauzată de ischemia miocardică persistentă, insuficienţa de pompă, dezechilibrul electrolitic, acidobazic și hipoxie [2, 4].
În faza inițială a STEMI sunt diagnosticate 5-20% de FV, 10-40% de TV și frecvent extrasistole ventriculare (EV), care precedează sau nu TV. FV primară tardivă poate surveni peste 1-6 săptămâni de la debutul IMA anterior extins, asociat cu blocuri complete de ram Hiss și tahicardie sinuzală (TS) persistentă [4]. TV poate fi nesusținută cu ritm ideoventricular accelerat, care în contextul unui STEMI nu prezintă markeri predictivi valizi pentru apariția FV timpurie și nu necesită tratament antiaritmic profilactic. TV susținută, cu deteriorare hemodinamică, survine în 3% din și necesită terapie urgentă [4, 5].
Fibrilația atrială (FA) este cea mai frecventă aritmie supraventriculară care apare la pacienți cu STEMI în 10-20% din cazuri, îndeosebi la vârstnici cu IMA extins și insuficiență cardiacă (IC), care se asociază cu mortalitate intraspitalicească înaltă și prezintă un prognostic rezervat [2]. Tahicardia sinuzală deseori este consecința hipercatecolaminemiei și a disfuncției de pompă în primele 24-48 de ore ale IMA. Tahicardia supraventriculară paroxistică (TSP) și fluterul atrial (FlA) se dezvoltă la 5% și 2% respectiv și cauzează creșterea consumului de oxigen și reducerea perfuziei coronariene, iar uneori poate produce disfuncție acută de pompă, necesitând tratament prompt [4].
Bradicardia sinuyală (BS) este frecventă în prima oră de la debutul IMA (30-40% din cazuri), dar incidența acesteia după 4 ore se reduce în jumătate. BS este asociată aproape întotdeauna infarctelor inferioare în 9-25% cazuri, care produc o stimulare vagală prin reflux Bezold Jarish sau prin reflex vaso-vagal [4]. Blocurile atrioventriculare (BAV), conform studiilor mari randomizate, survin în 7% din cazurile de STEMI [4, 7]. BAV au semnificație diferită, fiind asociate infarctelor inferioare sau anterioare.
Scopul lucrării a fost aprecierea incidenței dereglărilor de ritm și conductibilitate și a ratei de supraviețuire la pacienții cu infarct miocardic, complicat cu șoc cardiogen.
Material și metode
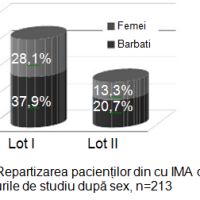
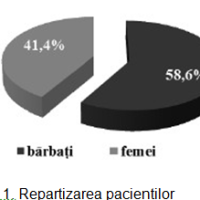
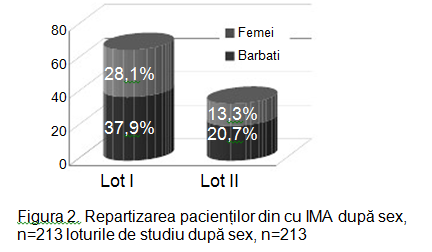
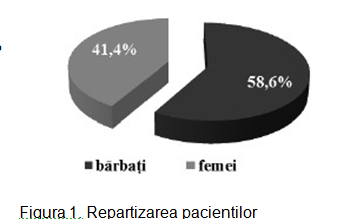
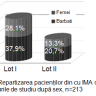
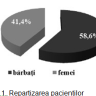
În studiu am inclus 213 pacienți cu vârsta medie de 64 ±0,1 ani, 58,6% bărbați și 41,4% femei. Pacienții au fost divizați în 2 loturi: I lot – cu dereglări de ritm și conductibilitate – 145 (68%) persoane; II lot – fără dereglări de ritm și conductibilitate – 68 (32%), cu evaluarea: datelor clinice, ECG, a markerilor lezării miocitare și neuroumorali. Rezultatele repartizării sunt ilustrate în figurile 1 și 2.
Rezultate obținute
Pacienții cu IMA au fost evaluați după tipurile IM cu prevalarea IMA 104 (48,8%), urmat de IM repetat – 62 (29,1%), IM supraacut – 24 (11,3%), IM recidivant – 5 (2,3%) și IM vechi – 18 (8,5%). Un alt obiectiv a fost cercetarea bolnavilor după localizarea IM și am obținut următorii indici: anterior extins – 97 (45,5%), posterior – 57 (26,8%), posterolateral – 18 (8,5%), anteroseptal – 15 (7%), inferior diafragmal – 11 (5,2%), anterior apical – 10 (4,7%) și lateral – 5 (2,3%).
Am analizat dereglările de ritm și conductibilitate la pacienții din studiu și am cercetat prevalarea disritmiilor în funcție de localizarea IMA, conform obiectivelor trasate. Am obținut următorii indici: în I lot au prevalat pacienți cu fibrilație atrială (FA) – 43 (32%), urmați de extrasistole supraventriculare (ESV) – 36 (24,6%), extrasistole ventriculare (EV) – 22 (14,9%), tahicardii sinuzale (TS) – 27 (20,1%), bloc de ram stâng f. Hiss (BRS) – 18 (12,7%), bloc de ram drept a f. Hiss (BRD) – 12 (8,2%), blocuri atrioventriculare (BAV) – 16 (11,2%) și bradicardie sinuzală (BS) – 15 (10,4%).
În IMA inferior diafragma l a prevalat fibrilația atrială în 4,5% cazuri, iar tahicardia sinuzală și fibrilația ventriculară – în raport egal de 1,5%. Tahicardia ventriculară s-a manifestat în 0,8%. Blocurile de ram drept al fasciculului Hiss au constituit un procent mai mic – 1,5%.
În IMA anterior extins au predominat fibrilația atrială (14,2%) și tahicardia sinuzală (11,2%), iar disritmiile ventriculare s-au întâlnit mai rar: extrasistolii ventriculare în 10,5% și fibrilație ventriculară în 6%.
Studiul ne-a demonstrat prevalența dereglărilor de conductibilitate în IMA posterior. Blocurile atrioventriculare au constituit 6%, blocurile de ram stâng versus de ram drept a fasciculului Hiss – 3% vs 0,8%. Bradicardia sinuzală am depistat-o în 3,7% cazuri. Complicațiile pacienților cu IMA din I lot au fost: edem pulmonar – 119 (55,9%), insuficiență respiratorie acută – 66 (31%), comă – 34 (16%), insuficiență renală acută – 22 (10,3%), tromboembolia arterei pulmonare – 17 (8%), ruptură de cord – 10 (4,7%) și edem cerebral – 4 (1,9%) cazuri.
Mortalitatea generală la pacienții din studiu a fost foarte înaltă – 122 (57,3%) cazuri, prevalând în lotul pacienților cu dereglări de ritm și de conductibilitate – 82 (61,2%) vs 40 (58%).
Concluzii
- La pacienții cu infarct miocardic, complicat cu șoc cardiogen, incidența aritmiilor și a blocurilor a fost foarte înaltă – 66%.
- În IMA anterior extins au prevalat aritmiile supraventriculare și cele ventriculare, iar în IMA posterior – bradiaritmiile și blocurile cardiace, cu rata de supraviețuire mai joasă.
- Cele mai frecvente complicații în IMA au fost: edemul pulmonar în 55,9%, insuficiența respiratorie acută în 31%, coma – în 16% și insuficiența renală acută – în 10,3% cazuri.
- Mortalitatea la pacienții cu IMA complicate cu șoc cardiogen a fost foarte înaltă 57,3%, cu predominarea pacienților cu disritmii – 61,2%.
Bibliografie
- 1. Braunwald E. Heart disease. vol. II, 2012.
- Bubenec Ș. Insuficiența cardiacă acută în terapia inten sivă. Ghid, 2008.
- Gherasim L. Boli cardiovasculare metabolice. 2011.
- Gingină C. Mic tratat de cardiologie. 2010, p. 609-620.
- Grosu A., ș.a. Infarctul miocardic acut. Protocol clinic național reactualizat. Chișinău, 2011.
- Hebbar A. ș.a. Managementul aritmiilor comune: aritmii ventriculare și aritmii în grupuri speciale de populație. In: Am. fam. medic., II, 2002, nr. 65 (12), p. 2491-2497.
- Rus M. ș.a. Diagnosticul de infarct miocardic utilizând troponina T, în comparație cu criteriile clinice și electrocardiografice, În: AMT, vol. II, nr. 3.
Lucia GÎRBU1,2, Alexandra GREJDIERU1, Victor COJOCARU1,
Liviu GRIB1, Gheorghe CAZACU1, Cornelia GUȚU-BAHOV1,
1USMF Nicolae Testemițanu,
2IMSP SCM Sfânta Treime