Limfomul gastric primitiv este o tumoră malignă rară, ce cuprinde mai puțin de 5% din totalul neoplasmelor gastrice. Cu toate acestea este cel mai frecvent limfom extraganglionar reprezentând 4-20% din totalul limfoamelor extraganglinare. Limfomul gastric afectează în general pacienții cu vârsta de peste 50 de ani, cu toate că există și pacienți cu debutul malignității la vârste mici, în decada a doua de viață. Media de vârsta la care debutează boala este între 60 și 65 de ani, bărbații fiind de 2-3 ori mai afectați comparativ cu femeile. Recent anumite studii au arătat că incidența limfomului gastric printre pacienții infectați cu virus HIV este în creștere, debutul bolii apărând la vârste tinere. [1]
Fiziopatologie
Limfoamele gastrice maligne se pot dezvolta fie ca tumoră primară ce pornește de la nivelul stomacului, fie ca metastază dintr-un limfom ce a afectat organismul sistemic. Stomacul este însă locul în care limfoamele ganglionare metastazează cel mai des, astfel apare limfomul gastric secundar. În general limfoamele sunt considerate ca fiind primare și ca având dezvoltare inițială la nivelul tractului gastrointestinal în momentul în care simptomele inițiale ale bolii sunt localizate la acest nivel determinând o afectare a funcției gastrointestinale.
Limfomul gastric primitiv se dezvoltă în marea majoritate de la nivelul mucoasei sau submucoasei din țesutul MALT (mucosa-associated lymphoid tissue = țesut limfoid asociat mucoasei) după o inflamație cronică produsă de infecția cu Helicobacter pylori.
Din punct de vedere histologic și imunohistochimic limfoamele gastrice dezvoltate pe MALT sunt în general limfoame non-hodgkin cu celule B. Asocierea dintre gastrita cronică cu Helicobacter pylori și limfomul MALT a fost confirmată de studii populaționale extinse, unde s-a dovedit imunologic existența infecției cu Helicobacter pylori la majoritatea pacienților cu limfom gastric MALT. Există și alte tipuri de limfom ce afectează stomacul, însă care nu se dezvoltă pe MALT și sunt rare. [4]
Clasificare histologică
Clasificarea histologică a limfoamelor se face în funcție de gradul de malignitate (deci de gravitatea acestuia). Gradul de gravitate poate fi mic, mediu sau înalt. În continuare este prezentată clasificarea histologică a limfoamelor gastro-intestinale. Acestea pot fi limfoame cu celule B sau limfoame cu celule T.
Limfoame gastrice cu celule В: limfoame MALT (ce cuprind limfoamele cu grad scăzut de malignitate și limfoame cu grad înalt de malignitate), bolile imunoproliferative ale intestinului subțire (cu grad mic de malignitate și cu grad înalt de malignitate), polipoza limfomatoasă, limfoamele Burkitt și limfoamele Burkitt-like.
Limfoamele gastrice cu celule T: limfomul cu celule T asociat enteropatiilor și limfomul cu celule T neasociat enteropatiilor.
O mare parte dintre limfoamele gastrice sunt din punct de vedere histologic limfoame cu celule mari, predominând cele cu celule В (limfocite B) mari. Reprezintă aproape jumătate din cazurile de limfom gastric primar. [5]
Din punct de vedere macroscopic limfoamele gastrice pot să fie ulcerate (cu ulcerații focale, multiple sau difuze), polipoide, granulonodulare sau infiltrative. Tipul ulcerativ tipic sau combinat cu alte tipuri de leziuni este cel mai frecvent.
Anatomopatologie □
Din punct de vedere microscopic limfoamele cu grad mic de malignitate sunt greu de diferențiat de pseudolimfoame. Pseudolimfoamele reprezintă infiltrarea mucoasei gastrice cu limfocite, care poate să apară la pacienții cu gastrită cronică și ulcer peptic. Pseudolimfoamele pot mima din punct de vedere clinic și endoscopic adenocarcinoamele gastrice sau limfoamele. Anatomopatologii diferențiază pseudolimfoamele de limfoame în funcție de anumite caracteristici histologice care indică modificările legate de malignitate (aparținând limfomului) precum leziunile limfoepiteliale accentuate (infiltrarea limfoidă a glandelor gastrice și a criptelor cu distrugere parțială a acestora), corpi Dutcher și atipii celulare moderate. în cazurile în care diferențierea între pseudolimfom și limfom nu s-a putut face histologic se apelează la studiul cu marked imunohistochimici și la biologie moleculară folosindu-se reacția polimerizării în lanț (PCR) care pot ajuta la stabilirea unui diagnostic concret. Studiile recente arată că marea majoritate a pseudolimfoamelor sunt de fapt limfoame adevărate cu grad mic de malignitate, prin urmare termenul de pseudolimfom urmează să fie abandonat. [4]
Aspect descoperit la examinarea endoscopică, cele mai multe tumori gastrice primare prezentându-se sub această formă. Leziunea poate apărea fie sub formă de țesut granulos fin până la țesut ulcerat infiltrativ. Endoscopic, diferențierea dintre limfoame și adenocarcinoame este destul de dificilă cu toate că limfoamele au tendința să crească mai mult în dimensiuni comparativ cu adenocarcinoamele și se dezvoltă multifocal, difuz de-a lungul mucoasei. Limfoamele gastrice implică cel mai frecvent antrul piloric și corpul gastric. Într-un studiu s-a descoperit că 46% dintre limfoame sunt localizate la nivelul corpului gastric cu toate că s-au raportat și cazuri care cuprindeau întregul stomac. Limfoamele avansate pot metastaza către zone extradigestive precum sistemul nervos central, osos, ficatul, rinichii, ovarele și plămânii. [1]
Tablou Clinic
Limfomul gastric primitiv are în general ca simptome inițiale durerea în zona epigastrică. Acestea sunt simptome nespecifice, cea ce duce la amânarea diagnosticului corect pe o perioadă destul de lungă care uneori poate ajunge la câțiva ani. Semnele și simptomele pot mima alte patologii abdominale precum ulcerul peptic, patologia vezicii biliare, pancreatita sau alte boli funcționale precum și alte tipuri de neoplasm gastric. Alte simptome frecvente sunt scăderea în greutate, greața, vărsăturile, meteorismul abdominal și indigestiile frecvente. Slăbiciunea musculară, transpirațiile profunde nocturne, icterul, febra și disfagia sunt simptome care apar mai rar. Majoritatea pacienților se prezintă târziu la medic tocmai datorită faptului că simptomele sunt nespecifice și presupun că au avut o indigestie sau prezintă un început de ulcer. Astfel la consultația inițială ajung după mult timp, în momentul în care simptomele persistă și devin deranjante, aceștia dezvoltând în general și anumite complicații ale bolii înaintea diagnosticului propriu-zis de limfom. 20-30% dintre pacienți se prezintă cu sângerări gastrointestinale precum hematemeză sau melenă (semnele unei hemoragii digestive superioare). Mai puțin frecvent acești pacienți se prezintă cu perforații și obstrucții gastrice.
Examinarea fizică este normală în general la 55-60% dintre pacienți. Semnele în general observate la examenul fizic sunt febra, hepatomegalia, splenomegalia, icterul și limfadenopatiile superficiale. 12% dintre pacienți prezintă ganglioni superficiali măriți. În stadiile avansate ale bolii sunt prezente și semnele malnutriției și deficitului de vitamine esențiale. [4], [1]
Diagnostic
Examenul clinic și cel radiologie sunt în general nespecifice.
Esofagogastroduodenoscopia (endoscopia digestivă superioară) și biopsia tumorii sunt metodele principale prin care se pune diagnosticul. Diagnosticul de limfom gastric cu grad mic de malignitate cu ajutorul biopsiei efectuată prin endoscopie este în general dificil de realizat la începutul bolii, întrucât caracteristicile histologice ale tumorii pot fi nespecifice. De aceea se indică efectuarea de endoscopii și biopsii nespecifice repetate, pentru a se ajunge la diagnosticul final.
Biopsiile multiple din diferite zone ale mucoasei gastrice sunt indicate deoarece aspectul endoscopic al tumorii poate varia foarte mult, de la modificări subtile ale mucoasei până la leziuni macroscopice evidente. Aceste modificări macroscopice sunt variabile și constă în: edemul mucoasei, mucoasa friabilă și sângerândă, focarele de eritem și hemoragie, țesutul de granulație, sângerarea de contact, eroziunile superficiale ale mucoasei cu formă neregulată și ulcerațiile. Biopsiile endoscopice repetate sunt obligatorii în cazul de suspiciune clinică a unei malignități dar prima biopsie este neconcludentă pentru diagnostic. De asemenea, dacă este posibil se poate face rezecția endoscopică a leziunii de mucoasă în cazul în care aceasta are dimensiuni mici și nu prezintă risc mare de sângerare.
Diagnosticul rapid endoscopic poate fi realizat prin detecția rearanjamentelor lanțurilor grele de imunoglobulină care apar în bolile limfoproliferative, țesutul obținut prin biopsie fiind supus unui PCR. Se recomandă ca mostrele de țesut biopsiat să fie supuse analizei histologice, imunohistochimice și studiilor de genotipare în vederea enunțării unui diagnostic cât mai corect și cât mai complet. [3]
Examinarea imagistică poate ajuta la enunțarea diagnosticului și la stabilirea extinderii leziunilor. Îngroșarea peretelui gastric, apariția de ulcere atipice și deformări ale țesuturilor, obstrucția și efectul de masă sunt aspecte radiologice sugestive pentru un proces malign la nivel gastric dar nespecifice pentru limfom.
Tomografia computerizată a abdomenului poate identifica îngroșarea peretelui gastric și leziunile înlocuitoare de spațiu în 85% din cazuri. În anumite cazuri pe scanări se pot vedea și imagini tipice care evidențiază îngroșarea omogenă a peretelui gastric, fapt care poate diferenția între limfom și adenocarcinom, adenocarcinomul gastric fiind cel mai frecvent tip de tumoră malignă a stomacului. Pe scanările CT, trei sferturi dintre limfoamele MALT cu grad scăzut de malignitate se prezintă sub forme infiltrative sau polipoide. La 50% dintre pacienți se detectează limfadenopatii viscerale.
Ecografia abdominală convențională poate avea valoare în identificarea procesului tumoral cu implicare gastrointestinală dar nu este specifică.
Rezonanța magnetică nucleară prezintă trăsături ale tumorii precum neregularitatea și îngroșarea pliurilor mucoase, infiltrarea neregulată a submucoasei, leziuni constrictive anulare, creștere tumorală exofitică, mase la nivel mezenteric și limfadenopatii retroperitoneale.
Ecoendoscopia este o tehnică foarte bună în ce privește stabilirea extinderii și invaziei leziunii. Ecoendoscopia poate diferenția între limfoame și carcinoame încă din primele stadii ale bolii, dar în stadii avansate limfoamele gastrice nu mai pot fi diferențiate atât de bine prin ecoendoscopie de adenocarcinoame deoarece ambele tipuri tumorale au aspect similar. Datorită numeroaselor metode performante de imagistică precum endoscopia digestivă superioară, tomografia computerizată, rezonanța magnetică nucleară și ecoendoscopia, rareori se mai supune pacientul chirurgiei deschise sau laparoscopiei exploratorii în vederea diagnosticului unei tumori gastrice. [4], [3], [5]
Stadializarea limfomului gastric
După stabilirea diagnosticului de limfom gastric primar, stadializarea este esențială pentru planificarea tratamentului. Este foarte important de asemenea să se diferențieze limfoamele cu implicare strict a stomacului de cele care au metastazat și limfoamele primare de limfoamele secundare.
Procesul de stadializare începe cu o examinare endoscopică și cu biopsii repetate la diverse nivele ale tractului gastrointestinal care sunt apoi trimise la laboratorul de anatomopatologie pentru a se stabili gradul de infiltrare microscopică a peretelui și care sunt zonele afectate. Se prelevează biopsii inclusiv din duoden pentru a se stabili dacă tumora a ajuns până la acel nivel.
Al doilea pas în stadializarea limfomului gastric îl reprezintă efectuarea unei radiografii toracice pentru a se evidenția eventuala invazie pulmonară sau mediastinală.
Scanările computer-tomografice ale toracelui, abdomenului și pelvisului permit evaluarea invaziei ganglionare supra și subdiafragmatice și stabilirea extensiei tumorii la nivel sistemic.
Ecoendoscopia poate fi utilizată pentru estimarea atât a gradului de invazie în perete cât și a implicării ganglionilor limfatici regionali. Ecoendoscopia este superioară scanării CT cu privire la emiterea de rezultate fals negative. Examinarea măduvei osoase ajută la determinarea prezenței sau absenței invaziei tumorale în os.
Efectuarea unei laringoscopii este utilă pentru excluderea implicării inelului Waldeyer care este frecvent invadat de celule maligne la pacienții cu limfom gastric. [1]
Stadializarea limfoamelor gastrice în funcție de criteriile Musshoff este următoarea:
Stadiul IE – Limfom cu extindere limitată la nivelul stomacului.
Stadiul IIE1 – Implicarea stomacului și a ganglionilor limfatici învecinați
Stadiul IIE2 – Implicarea stomacului și a altor ganglioni limfatici subdiafragmatici.
Stadiul III – Invazia stomacului și a ganglionilor limfatici supradiafragmatici și subdiafragmatici.
Stadiul IV – Invazia pe cale hematogenă cu afectarea stomacului și a altor organe și țesuturi extralimfatice.
La aceste stadii se pot adăuga și următoarele prescurtări: E- invazie extranodală, S- invazia splinei, A- asimptomatic, B- simptomatic.
S-au folosit diferite sisteme de stadializare, cea mai folosită fiind stadializarea Ann Arbor a limfoamelor primare modificată de către Musshoff. [5]
Tratament
Tratamentul pentru limfomul gastric dispune de modalități multiple și nu există la momentul actual un protocol strict în ce privește aplicarea lor.
Opțiunile de tratament sunt însă în toate cazurile dependente de clasificarea histologică și de stadiul în care se află boala. Anumite centre recurg doar la chirurgie în timp ce alte centre sunt adeptele tratamentului non-chirurgical cu ajutorul chimioterapiei și radioterapie. [2]
Tratament chirurgical
Rezecția chirurgicală agresivă a tumorii este în momentul actual principalul tratament și cel mai utilizat, întrucât cu ajutorul chirurgiei se pot colecta mostre mari de țesut pentru analiza anatomopatologică, se explorează minuțios abdomenul, se reduce încărcătura tumorală prin excizii ample și este utilizată în scop curativ în cazul în care boala nu se află în stadiu avansat. La momentul actual se reconsideră efectuarea gastrectomiei radicale (exciziei complete a stomacului, splinei și a tuturor ganglionilor limfatici perigastrici) ca tratament de bază în limfom, aceasta nefiind considerată necesară în toate cazurile bolii. În stadiile inițiale ale bolii se poate reduce și la gastrectomie parțială.
Părerile sunt însă contradictorii. Anumiți autori prezintă gastrectomia totală ca tratament curativ chiar din stadiile inițiale ale bolii împreună cu excizia tuturor ganglionilor limfatici regionali în timp ce alți autori consideră că în stadiile IE și IIE poate fi efectuată și gastrectomia parțială sau tratament conservator cu chimioterapie și radioterapie, întrucât au fost obținute rezultate foarte bune în ce privește supraviețuirea la 5 ani în urma tratamentului conservator. Însă, la momentul actual tot chirurgia radicală este cea mai utilizată metodă de tratament, alături de tratamentul infecției cu Helycobacter pylori. [2], [4]
Mortalitatea și morbiditatea tratamentului chirurgical sunt similare cu cele înregistrate în urma aplicării tratamentului non-chirurgical (chimioterapie și radioterapie) pentru limfoamele gastrice în stadiile I și II. În aceste stadii nu este indicată chirurgia agresivă deoarece aceasta duce la creșterea morbidității și la scăderea dramatică a calității vieții pacientului după operație. La o rată de rezecabilitate a stomacului între 60 și 88% s-au înregistrat rate de supraviețuire la 5 ani între 50 și 87%. Chirurgia radicală a bolii avansate a fost asociată cu rate mai mare de morbiditate și mortalitate și rate mici de răspuns la tratament între 6 și 40%. Mortalitatea postoperatorie în cazul tumorilor avansate este între 3 și 25% și chirurgia paleativă având rate ridicate ale mortalității.
Chirurgia paleativă se face în scopul reducerii durerii pacientului și ameliorării simptomelor legate de masa tumorală precum și în vederea controlării hemoragiilor asociate cu alte tipuri de tratament. Se fac proceduri de rezecție parțială a tumorii și de hemostază.
Terapia combinată
Terapia multimodală ce combină rezecția chirurgicală a tumorii cu chimioterapia și ocazional cu radioterapia este acceptată ca modalitate principală de tratament în cele mai multe centre. Utilizarea ei a crescut simțitor rata de supraviețuire la 5 ani a pacienților diagnosticați cu limfom gastric. Chirurgia cu intenție de radicalitate asociată cu chimioterapie a determinat îmbunătățirea simțitoare a ratei de supraviețuire și a răspunsului la tratament comparativ cu utilizarea doar a chimioterapiei. Chimioterapia folosită în vederea îmbunătățirii rezultatului chirurgiei radicale și scăderii ratei de recidivă tumorală poartă numele de chimioterapie adjuvantă. Cele mai noi studii recomandă asocierea chirurgiei radicale cu chimioterapia adjuvantă ca tratament de primă intenție pentru limfoamele gastrice indiferent de gradul de malignitate. Un studiu chinez arată că utilizarea chimioterapiei postoperatorii determină creșterea ratelor de supraviețuire post-rezecție chirurgicală. Un studiu prospectiv realizat în Franța vine cu o estimare foarte optimistă, aproximând rata de supraviețuire postoperatorie la pacienții cu limfom cu grad înalt de malignitate care au fost supuși apoi chimioterapiei, iar mai apoi chimioterapiei adjuvante la 99-100%. Superioritatea chirurgiei combinate cu chimioterapia a fost observată în foarte multe studii, arătându-se că pentru stadiile IE și IIE terapia combinată crește șansele de supraviețuire la 86-94%. Ratele de supraviețuire sunt mai mari decât cele ale pacienților supuși exclusiv intervenției chirurgicale radicale, chimioterapia adjuvantă reducând foarte mult riscul de metastazare al tumorii deoarece în ciuda exciziei ei cu limite de siguranță oncologice, riscul existenței metastazelor microscopice în țesutul rămas neexcizat este încă ridicat. Terapia combinată, pe lângă faptul că crește rata de supraviețuire a fost asociată și cu o rată mult mai mică de recidivă și metastazare. [1], [4]
Stadiile inițiale ale bolii indiferent de tipul histologic pot fi controlate prin chimioterapie sau prin chimioterapie asociată cu radioterapie. Avantajul în aceste cazuri este prezervarea stomacului și evitarea morbidității și mortalității asociate cu chirurgia. Pe de altă parte chirurgia este singura modalitate sigură care poate asigura controlul bun al bolii din cauză că doar chirurgical medicul poate fi sigur că tumora a fost excizată și a dispărut complet. Prin urmare și în stadiile inițiale ale bolii se recurge la terapia combinată cu chirurgie și chimioterapie adjuvantă.
Un interes ridicat este alocat limfoamelor maligne MALT întrucât regresia tumorii a fost raportată în anumite cazuri în care s-a reușit eradicarea infecției cu Helicobacter pylori. Un studiu ce a cuprins 120 de pacienți cu limfom gastric MALT în stadiu incipient care au fost tratați cu terapie anti Helicobacter pylori ce a cuprins amoxicilină și omeprazol s-a raportat o rată de remisiune de 81%, alți 9% dintre pacienți având o remisiune parțială. Un alt studiu care a tratat 233 de pacienți cu antibiotic a raportat remisiune completă la 62% dintre aceștia și remisiune parțială la 12% după 6 luni. După 40 de luni de urmărire a acestor pacienți 13% au înregistrat recidiva limfomului gastric. Nu se cunoaște încă ce stadii ale limfomului gastric răspund la terapia de eradicare a Helicobacter pylori însă se crede că eradicarea acestui microorganism este o opțiune de tratament care trebuie luată obligatoriu în considerare.
Rezecția chirurgicală, radioterapia,chimioterapia și combinația acestora sunt toate modalități de tratament eficace. Radioterapia a fost încercată ca formă locală de tratament la un număr mic de pacienți, înregistrându-se o rată de supraviețuire de 93%. La acestea se adaugă terapia de eradicare a Helycobacter pylori cu antibiotice. [5], [1]
Prognostic
Limfomul gastric are un prognostic bun în următoarele condiții: limfom gastric cu grad mic de malignitate, pacienții cu vârsta sub 65 de ani, rezecția chirurgicală cu respectarea marginilor de siguranță oncologică și remisiune inițială completă a tumorii.
În boala avansată un prognostic bun poate fi atins în cazul în care limfomul gastric are un grad mic de malignitate și răspunde bine la chimioterapie și radioterapie. Prognosticul limfomului gastric este similar cu cel al limfoamelor extradigestive.
Stadiul bolii joacă de asemenea un rol foarte important în ceea ce privește prognosticul, alături de gradul histologic de malignitate. Este ușor de dedus faptul că o boală aflată într-un stadiu incipient va avea un prognostic mult mai bun comparativ cu cea în stadiul II sau III.
Ratele de supraviețuire la 5 ani sunt 91% pentru limfoamele cu grad redus de malignitate și între 56-73% pentru limfoamele cu grad înalt de malignitate.
În concluzie, datorită rarității foarte mari a limfomului gastric, foarte multe aspecte în ce privește stadializarea și mai ales tratamentul bolii sunt controversate și nu există un protocol de tratament bine stabilit pentru acest tip de limfom. De cele mai multe ori pacienții se prezintă la medic târziu, cu o boală în stadiu avansat însă metodele noi de diagnostic ajută la emiterea unui diagnostic corect chiar din stadiile incipiente. Majoritatea limfoamelor gastrice sunt de tip MALT. [3], [4]
Cel mai bun tratament pentru limfomul gastric nu a fost încă stabilit dar pentru boala avansată aflată în stadiu III sau IV, cea mai bună modalitate terapeutică se consideră a fi combinarea chimioterapiei cu radioterapia deoarece chirurgia este asociată cu o mortalitate și morbiditate semnificativă. Cea mai bună modalitate de tratament pentru limfoamele în stadiile I și II este rezecția chirurgicală completă a tumorii. Pentru limfoamele MALT se adaugă în tratament și eradicarea infecției cu Helicobacter pylori. Se așteaptă noi triajuri randomizate care să clarifice care dintre modalitățile de tratament, conservator, chirurgical sau combinat este mai eficace pentru tratamentul limfomului gastric localizat, fără metastaze. [5], [1]
Bibliografie
- Primary gastric lymphoma-Pubmed resources,
Link: http://www.ncbi.nlm.nih.gov/books/NBK6966/
- Mucosa- Associated Lymphoid Tissue- Medscape,
Link: http://emedicine.medscape.com/article/207891-overview
- Primary gastric lymphoma, Non-Hodgkins lymphomas-WebMd,
Link: http://www.webmd.com/cancer/non-hodgkins-lymphoma/lymphoma-gastric non-hodgkins-type
- The primary gastric lymphoma-surgical oncology net,
Link: http://www.surgical-oncology.net/lymphoma2.htm
- Pathogenesis and treatment- British Journal of Haematology,
Link: http://onlinelibrary.wiley.eom/doi/10.1111/j.1365- 2141.2006.06444.x/pdf
Caz clinic:
Pacient: D. G 57 ani S: masculin, mediu rural, fumător, grupa sanguină: A (II) Rh (+) pozitiv, internat Clinica Chirurgie ,, Constantin Țîbîrnă,, secția chirurgie aseptică a SCM „Sfânta Treime” 08.08.2017;
Acuze: inapetență, dureri epigastrale, vărsături postprandiale precoce, scădere ponderală (-20kg/2 luni), incapacitatea tranzitului alimentar (totală alimente solide, cu dificultate pentru lichide);
Diagnosticul la internare: Stenoza corpului gastric după administrare de substanță toxică (anhidrida);
21.06.-12.07.2017 internat în secția toxicologie cu diagnosticul: Intoxicație acută cu substanță corozivă. Combustie chimică a mucoasei tractului digestiv. Hemoragie gastrică Forest II-B;
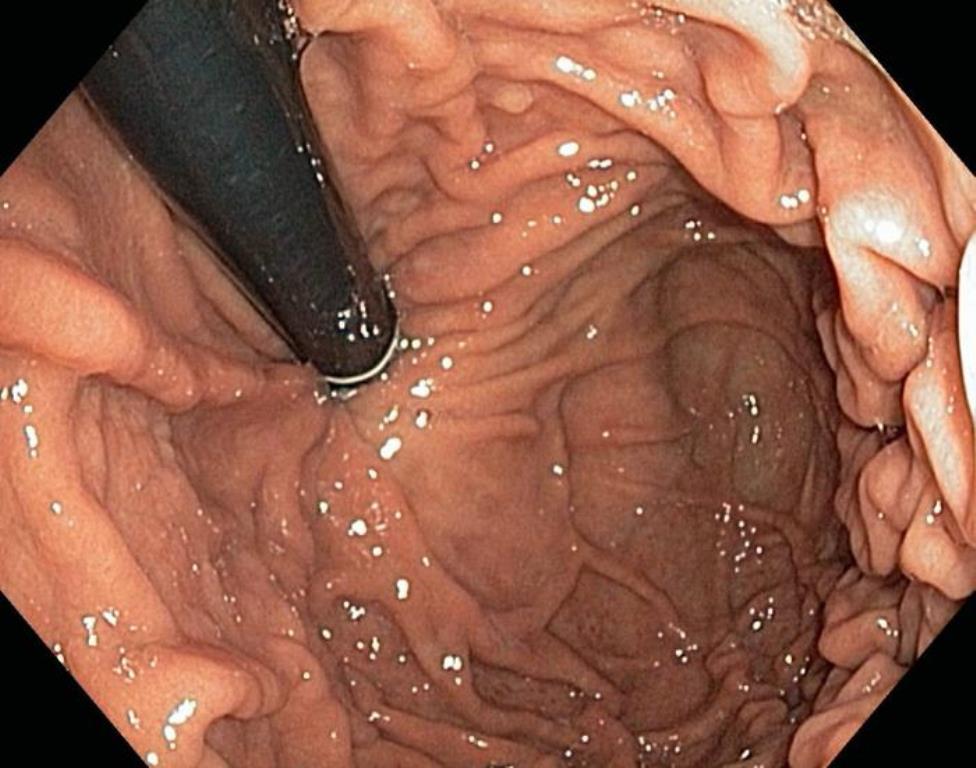
FEGDS: Combustie chimică a mucoasei TD. Eso-gastrită necrotică totală. Hemoragie Forest II-B
FEGDS peste 2 luni: Esofagul normal. Gastrită chimică cu regenerare incompletă. Nu este posibil de pătruns în corpul stomacului cu aparatul. Stenoză subtotală a corpului gastric.
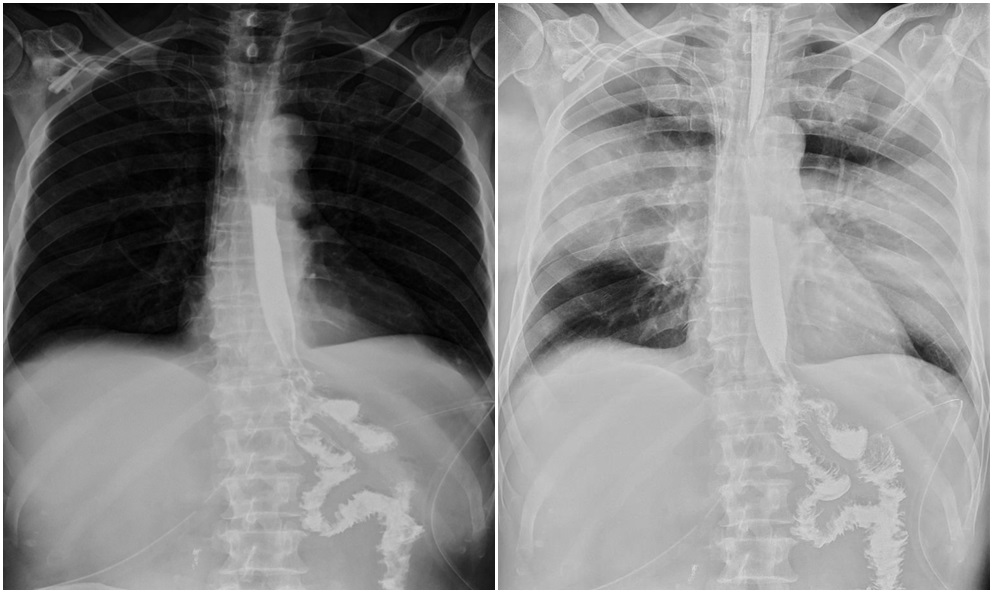
Radioscopia preoperatorie a tractului digestiv superior cu radiofarmaceutic (stenoză qwasitotală a corpului gastric):
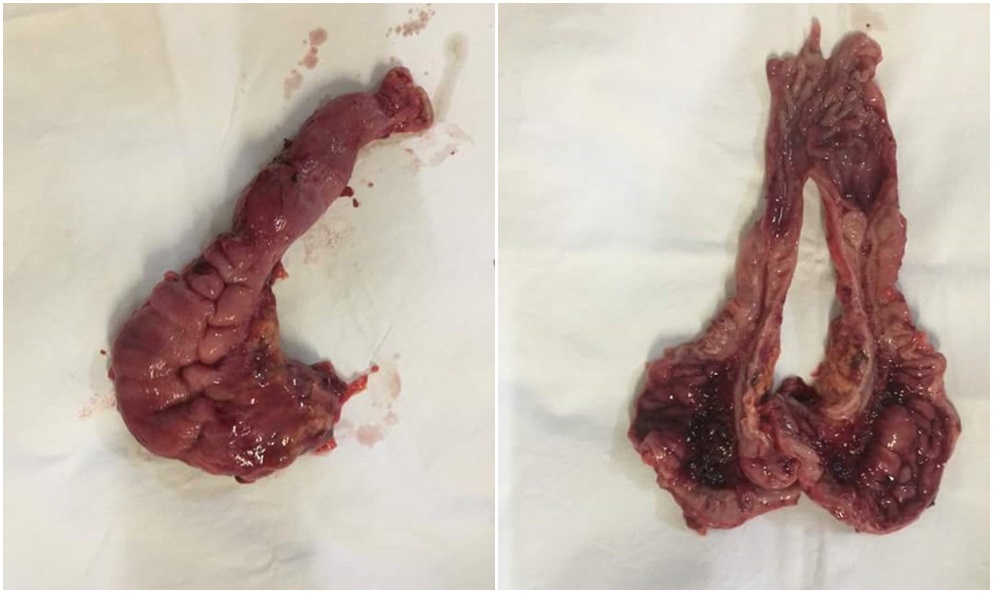
Operație10.08.2017: Laparotomie medio-mediană. Gastrectomie totală cu eso-enteroanastomoză și entero-enteroanastomoză. Splenectomie. Dreanarea cavității peritoneale.
Macropreparat (integru, secționat):
Evoluție postoperatorie: A VI-a zi postoperator: Alterarea stării generale a pacietului. T- 38- 38,5 C. Semne de iritații peritoneale pozitive; 16.08.2017. Relaparotomie. Suturarea defectului (dehiscenței) peretelui anterior de anastomoză eso-jejunală. Sanarea si drenarea cavității peritoneale.
Diagnostic postoperator: Dehiscență a peretelui anterior a eso-jejunoanastomozei. Peritonită purulentă generalizată.
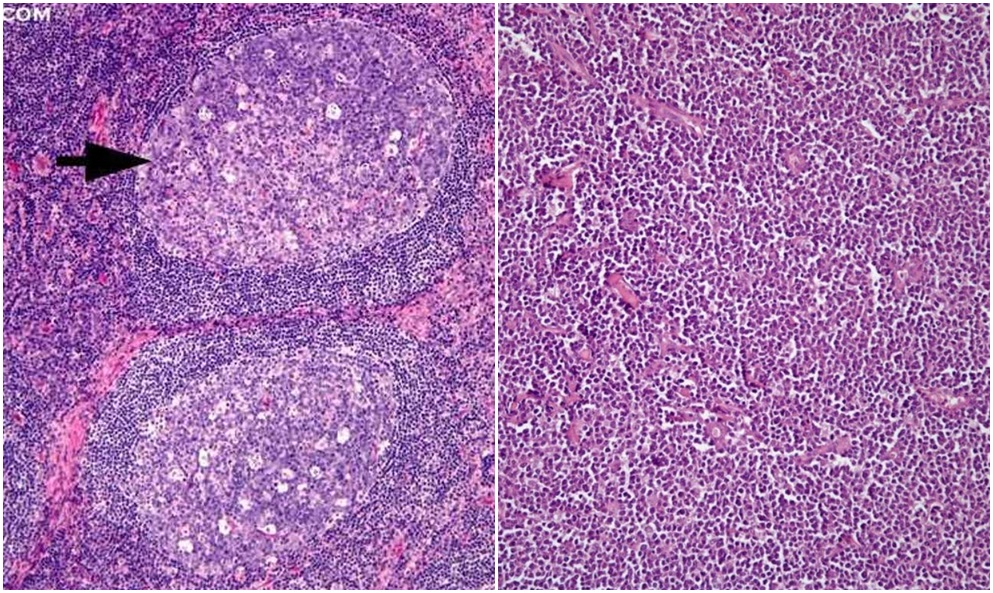
Concluzie patomorfologică: Gastrită hipertrofică cu focare de hiperplazie al epiteliului glandular. Intr-o serie de secțiuni sunt focare în care este pierdută arhitectonica normală a folicolilor limfoizi cu prezenta celulelor polimorfe atipice printre care prevalează celule limfocitare. Totodată se apreciază infiltrate celulare și la nivelul stratului submucos și muscular – suspecție la Limfom Non-Hodgkin. Urmează de a se determina histogeneza procesului patologic în cadrul Institutului Oncologic.
Radioscopia postopertaorie a tractului digestiv superior cu radiofarmaceutic (a 20-a zi postoperator cu tract digestiv reconstruit):
FEGDS (05.09.2017): esofagul permeabil. Anastamoza e liberă, permeabilă. Semne de stenoză sau malformație nu sunt.
Echipa operatorie:
Gheorghe STRAJESCU – conferențiar universitar, doctor în științe medicale, vice-director profil chirurgie a SCM „Sfânta Treime”;
Petru BUJOR – profesor universitar, doctor habilitat în științe medicale, șef Clinică Chirurgie ”Constantin Țîbîrnă”;
Alina BOTNARENCO – medic rezident chirurg;
Lilia ȚÎGANCIUC – sef secție Anesteziologie a SCM „Sfânta Treime”, medic-anesteziolog.